¿Qué dice la primera ley de la termodinámica?: Primera ley de la termodinámica: todo lo que debes saber
Si eres un estudiante de física o simplemente un apasionado por la ciencia, seguramente has escuchado hablar de la primera ley de la termodinámica. Esta ley es una de las más importantes en el campo de la termodinámica y es fundamental para entender cómo funcionan los procesos de transformación de la energía.
En este artículo, vamos a profundizar en todo lo que debes saber sobre la primera ley de la termodinámica. Desde su definición y sus implicaciones, hasta su relación con otros conceptos de la física. También responderemos a algunas preguntas frecuentes que suelen surgir sobre esta ley.
- ¿Qué es la primera ley de la termodinámica?
- ¿Cuál es la implicación de la primera ley de la termodinámica?
- ¿Cómo se relaciona la primera ley de la termodinámica con el trabajo?
- ¿Cómo se relaciona la primera ley de la termodinámica con el calor?
- ¿Cómo se aplica la primera ley de la termodinámica en la vida cotidiana?
- ¿Cuál es la diferencia entre la primera ley de la termodinámica y la segunda ley de la termodinámica?
- ¿Por qué es importante la primera ley de la termodinámica?
- ¿Qué es un sistema aislado?
- ¿Qué es la energía interna de un sistema?
- ¿Cómo se puede calcular la energía interna de un sistema?
- ¿Qué es la ley cero de la termodinámica?
- ¿Qué es la termodinámica?
¿Qué es la primera ley de la termodinámica?
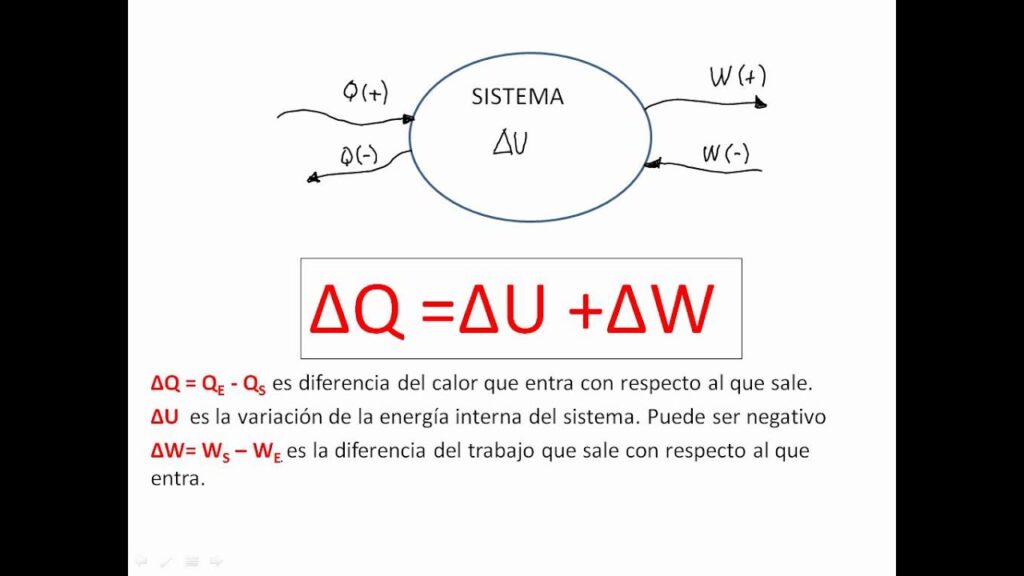
La primera ley de la termodinámica es una ley fundamental de la física que establece que la energía no se crea ni se destruye, solo se transforma. En otras palabras, la cantidad total de energía en un sistema aislado es constante.
Esta ley se basa en la conservación de la energía, un principio fundamental en la física que establece que la energía no puede ser creada ni destruida. Solo se puede transferir de un lugar a otro o transformarse de una forma a otra.
¿Cuál es la implicación de la primera ley de la termodinámica?
La implicación más importante de la primera ley de la termodinámica es que la energía en un sistema aislado es constante. Esto significa que si un sistema recibe energía, esta energía debe provenir de algún otro lugar. De la misma forma, si un sistema pierde energía, esta energía debe ir a parar a otro lugar.
Esta ley también nos permite entender cómo se pueden transformar diferentes formas de energía. Por ejemplo, si un objeto se mueve a una velocidad constante, tiene energía cinética. Si este objeto se detiene, su energía cinética se transforma en energía térmica debido a la fricción.
¿Cómo se relaciona la primera ley de la termodinámica con el trabajo?
La primera ley de la termodinámica también se relaciona con el concepto de trabajo. El trabajo se define como la energía transferida a un objeto para moverlo a través de una distancia determinada. Cuando se aplica una fuerza a un objeto y este se mueve, se está realizando trabajo.
La relación entre la primera ley de la termodinámica y el trabajo es que la energía transferida en forma de trabajo no se pierde. Si se realiza trabajo sobre un sistema, la energía transferida se convierte en energía interna, que es la energía que poseen las moléculas del sistema.
¿Cómo se relaciona la primera ley de la termodinámica con el calor?
La primera ley de la termodinámica también se relaciona con el calor, que es una forma de energía que se transfiere debido a una diferencia de temperatura. El calor fluye desde un objeto caliente a uno frío hasta que ambos objetos alcanzan la misma temperatura.
La relación entre la primera ley de la termodinámica y el calor es que el calor transferido a un sistema se convierte en energía interna, que es la energía que poseen las moléculas del sistema.
¿Cómo se aplica la primera ley de la termodinámica en la vida cotidiana?
La primera ley de la termodinámica se aplica en muchos aspectos de la vida cotidiana. Por ejemplo, cuando cocinamos algo en una estufa, estamos transfiriendo energía térmica al alimento para que se cocine. La energía térmica proviene de la combustión de gas natural o electricidad.
Otro ejemplo es cuando se conduce un automóvil. El motor del automóvil convierte la energía química del combustible en energía cinética, lo que permite que el automóvil se mueva.
¿Cuál es la diferencia entre la primera ley de la termodinámica y la segunda ley de la termodinámica?
La primera ley de la termodinámica establece que la energía no se crea ni se destruye, solo se transforma. La segunda ley de la termodinámica establece que la entropía de un sistema aislado siempre aumenta con el tiempo.
La entropía se refiere al grado de desorden o caos en un sistema. La segunda ley de la termodinámica establece que en un sistema aislado, la entropía siempre aumenta con el tiempo. Esto significa que la energía en un sistema aislado se vuelve cada vez menos utilizable.
¿Por qué es importante la primera ley de la termodinámica?
La primera ley de la termodinámica es importante porque nos permite entender cómo se comporta la energía en diferentes sistemas. Gracias a esta ley, podemos entender cómo se transforma la energía y cómo se puede transferir de un lugar a otro.
Esta ley también es fundamental para entender el funcionamiento de muchos procesos industriales y tecnológicos. Por ejemplo, en la producción de electricidad, se utiliza la primera ley de la termodinámica para entender cómo se puede transformar la energía térmica en energía eléctrica.
¿Qué es un sistema aislado?
Un sistema aislado es un sistema que no intercambia energía ni materia con su entorno. En otras palabras, un sistema aislado no recibe energía o materia del exterior y tampoco las transfiere hacia el exterior.
¿Qué es la energía interna de un sistema?
La energía interna de un sistema se refiere a la energía total que poseen las moléculas del sistema. Esta energía incluye la energía cinética y la energía potencial de las moléculas.
La energía interna de un sistema puede cambiar si se realiza trabajo sobre el sistema o si se transfiere calor al sistema. Si se realiza trabajo sobre un sistema, la energía transferida se convierte en energía interna. Si se transfiere calor al sistema, la energía térmica se convierte en energía interna.
¿Cómo se puede calcular la energía interna de un sistema?
La energía interna de un sistema se puede calcular sumando la energía cinética y la energía potencial de todas las moléculas del sistema. En la práctica, este cálculo puede ser muy complejo debido a la gran cantidad de moléculas que pueden estar presentes en un sistema.
En la mayoría de los casos, es más fácil medir la cantidad de calor que se transfiere a un sistema o la cantidad de trabajo que se realiza sobre un sistema para calcular la variación de la energía interna.
¿Qué es la ley cero de la termodinámica?
La ley cero de la termodinámica establece que si dos sistemas están en equilibrio térmico con un tercer sistema, entonces también están en equilibrio térmico entre ellos.
Esta ley es importante porque nos permite definir la temperatura y entender cómo se transfiere el calor entre diferentes objetos.
¿Qué es la termodinámica?
La termodinámica es una rama de la física que estudia las propiedades de la materia y la energía en sistemas físicos macroscópicos. La termodinámica se enfoca en el estudio de los procesos de transferencia de energía y de cómo se pueden transformar diferentes formas de energía.
La primera ley de la termodinámica es una ley fundamental de la física que establece que la energía no se crea ni se destruye, solo se transforma. Esta ley es fundamental para entender cómo se comporta la energía en diferentes sistemas y procesos. Además, es importante para entender muchos aspectos de la vida cotidiana y procesos industriales y tecnológicos.

Deja una respuesta